crc 须知!试验用药品管理-凯发k8旗舰厅
-
标准:遵循gcp的原则以及试验药物管理的sop。
-
执行:
(1)委派符合资格的人员。
(2)相关人员进行试验药物管理培训。
(3)所有药品相关的试验资料应当被准确记录,妥善保存。
-
检查/核实:
(1)试验药物的制备应当符合临床试验用药品生产质量管理相关要求。
(2)试验药物的使用应当符合试验方案。
❖ 申办方/cro
负责研究药物的生产、供应、包装、运输,具体包括:
-
保证药品质量合格(gmp生产、易于识别、正确编码)。
-
建立试验药物管理和记录系统。
-
负责向研究中心提供试验药物(安全送达药物、保存相关文件、回收试验药物、处置未使用试验药物)。
❖ 研究者
熟悉了解试验药物,负责试验药物的使用;掌握临床试验进行期间发现的所有与药物有关的信息。研究者必须保障:
-
所有研究药物仅用于临床试验的受试者。
-
剂量与用法需要遵照试验方案。
-
剩余的试验用药退回申办方。
-
由专人管理研究药物。
❖ crc或其他指定人员
(一)负责药物管理的实际工作,需要具备药物管理资格:
-
具备相应的专业背景(药学/护理学等)。
-
获得研究者的授权。
-
接受研究药物管理的培训。
(二)负责药物管理的专项工作:
-
药物管理的过程均须记录。
-
接受相关人员对药物管理工作的检查。
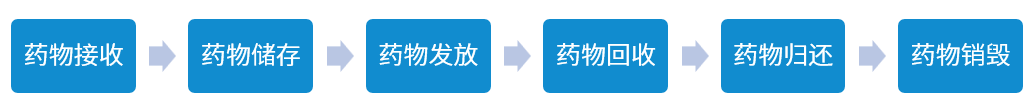
❖ 试验用药物的接收
(一)在试验开始前
crc应确认试验用药品存放的地点、环境、接收地址、接收人及凯发k8旗舰厅的联系方式。
(二)试验用药品到达后
-
crc (或协助药物管理员)接收,并与药物运单核对,包括药物名称、数量、药物批号、药物编号、规格、剂型、有效期等。
-
crc (或协助药物管理员)填写药物接收的表格及药物库存表。
-
crc (或协助药物管理员)负责保管运送药物的温度计,确保仪器完好可用。
-
crc (或协助药物管理员)核对完所有药物信息并确认无误后,立即通过ivrs/iwrs等途径确认接收药物,收到确认文件后再次与药物信息核对,无误后打印签字,并保存。
❖ 试验用药物的储存
-
crc (或协助药物管理员)对试验用药品保存的环境应定期进行核查:干燥、通风、整洁、卫生、无污染及污染源,并做好防火、防尘、防潮、防虫及防鼠等相应管理工作。
-
crc应确认试验用药品按项目存放,专人专柜加锁保管,并根据方案要求进行药物储存。
-
crc (或协助药物管理员)依照方案要求记录温度、湿度,若发现温、湿度异常,应及时与监查员沟通,并协助药物管理员寻找原因并解决,记录储存条件偏离的时间、所储存的药品数量、药物编号等,报方案偏离。
-
crc (或协助药物管理员)应定期检查药物有效期,发现过期药物应及时与药物管理员及监查员联系;针对过期药物,按照申办方的要求处理。
-
crc应确认有效药物与过期药物、回收药物与未分发药物均已分开放置,并有明显标注。
-
crc (或药物管理员)应确保一定数量的库存。
-
需要特殊保存条件的药物,应根据相应要求制定药物保存的核查规定。
❖ 试验用药物的发放
-
分发药物应由被授权的药物管理员或crc进行,这些人员在试验开始前应接受并完成药物管理的相关培训。
-
通过随机系统获取研究药品编号时,crc需首先输入项目号、中心号、受试者编号、性别、出生日期、访视日期、访视周期、剂量调整等信息,然后确认输入的信息是否准确,在获取确认文件后再次确认。
-
crc (或协助药物管理员)应根据药品发放的确认文件,及医嘱或处方领取相应编号的试验用药品,并及时在“药品发放回收登记表”记录。
-
分发试验用药品前,crc (或药物管理员)应与研究者或指定研究人员双方再次核对药物编号、受试者编号、随访周期等信息是否与确认文件中的信息一致,确保药品的准确发放。发给受试者时,由受试者确认后在签收单上签字,即发药的每个步骤都需要确认。
-
crc (或协助药物管理员)提醒受试者剩余的试验用药品(包括无论何种原因未使用的药物)需要回收,必须在下一次随访时将剩余药物及用药日记卡带回研究中心。
❖ 试验用药物的回收
-
crc(或协助药物管理员)回收受试者每次的剩余药物、药盒或药板,应认真清点并记录在“药物发放回收记录表”中。
-
crc若发现剩余药量与实际应归还的数量不一致,或者发现服药日记卡记录的数量或时间点未符合方案要求时,需向受试者进行确认,了解是否有多服或漏服试验用药品,并再次指导受试者正确服药以及告知其正确服药的重要性,同时提醒研究者将真实情况记录在病历中。
❖ 试验用药物的归还
-
剩余的试验药物应返回申办方,封箱寄回(其他处置方法应妥善记录)。
-
必须记录内容包括:日期、数量、批号、有效期(如有)、分配的试验用药和受试者编码。
❖ 试验用药物的销毁
-
试验过程中或结束后,crc (或药品管理员)应确认需要销毁的试验用药品,核对其数量与“药品发放回收登记表”记录的受试者归还数量是否一致,同时做好销毁记录。
-
crc (或药物管理员)协助监查员将需收回的试验用药品打包,监查员填写销毁相关表格。药物管理员与cra双人核对签字,原件一式两份,一份由中心存档,一份由申办方存档。若为快递运送,需存档快递单。
-
如在研究中心销毁,crc (或药物管理员)保存申办方的销毁委托函,并对销毁药物的申办方、项目号、药物名称、数量、销毁时间、地点、参加人员等进行记录,原件式两份,一份由中心存档, 一份由申办方存档。
-
非试验相关人员不得接触试验用药品。
-
试验用药品必须按照方案的要求妥善保存。
-
试验用药品的接收、分发、回收、清点、销毁等必须有书面记录。
-
试验用药品可由crc直接管理及发放。
-
试验用药品储存标签应摆放合理,以便观察。
-end-


转载声明:未经本网或本网权利人授权,不得转载、摘编或利用其他方式使用上述作品。已经本网或本网权利人授权使用作品的,应在授权范围内使用,并注明“来源:新领先医药科技”。
 hotline服务热线:010-61006450
hotline服务热线:010-61006450


 010-61006450
010-61006450 联系地址:
联系地址: 技术市场部邮箱:
技术市场部邮箱: 北京新领先
北京新领先 新领先药讯
新领先药讯 010-61006450
010-61006450
